跟著動圖,「星標」賽柏藍器械,將自動成為VIP讀者,定期有福利喔~ ? 來源: 醫療 器械經銷商聯盟 “ 合規合法仍是第一要義 ” 經營生產不合規,醫械企業被罰百萬余元 日前,天津市藥監局最新發布了一則行政處罰決定書。 處罰書中顯示,2020年7月10日天津市
日前,天津市藥監局最新發布了一則行政處罰決定書。
處罰書中顯示,2020年7月10日天津市藥品監督管理局執法人員接舉報后對某醫療設備有限公司進行現場檢查,發現該公司生產車間中正在生產的GD2000型連體式牙科綜合治療機中牙科病人椅所使用的驅動元器件為傳動電機。
經核實,該產品注冊時所使用的驅動元器件為液壓傳動。當事人擅自將驅動部件由液壓傳動變更為電機傳動,不符合經注冊的連體式牙科綜合治療機產品技術要求,違反了《醫療器械監督管理條例》第二十四條第一款的規定。
另,天津市藥品監督管理局于2020年9月4日對當事人生產經營的GD2000型連體式牙科綜合治療機使用說明書進行調查,發現產品說明書中適用范圍“是用于各種牙科診斷和治療的醫療器械。”與經備案的說明書適用范圍“連體式牙科綜合治療機是供醫療機構口腔醫學專業常規口腔檢查,診斷,治療用。”內容描述不一致,產品說明書中腳踏控制系統的部件圖片及操作說明等內容與經備案的說明書內容不一致。上述行為構成了生產說明書不符合規定的連體式牙科綜合治療機的要件,違反了《醫療器械監督管理條例》第二十七條第一款的規定。
鑒于當事人積極主動配合提供有關賬冊、票據、記錄等證據材料,并主動采取召回措施,降低了產品的潛在風險。最終,依據《醫療器械監督管理條例》第六十六條第一款第二項的規定,天津市藥品監督管理局責令當事人改正違法行為,處罰款69.19萬元。同時,依據《醫療器械監督管理條例》第六十七條的規定。責令當事人立即改正說明書與經備案的說明書內容不一致的行為,并給予2萬元罰款的行政處罰。2項罰款合計71.19萬元。
事實上,除了上述市監局發布的行政處罰外,近日中國醫療器械風險預警平臺還發布了醫療器械企業風險預警提示數據。
平臺數據來自合法途徑獲取的公開數據,對5年來的相關數據按不同權重賦值,從負面傳播、過度宣傳、投訴舉報、產品缺陷、經營風險、處罰訴訟、生產違規等多個維度進行建模。
其中,多家公司均在近期被媒體曝光其產品存在質量問題。
早在今年的1月初,中國健康傳媒集團輿情監測中心發布的風險指數排名前十的企業中,里面也曾包含不少“熟面孔”。
值得注意的是,由于監測平臺數據滾動更新,醫療器械企業風險預警提示也是動態更新。
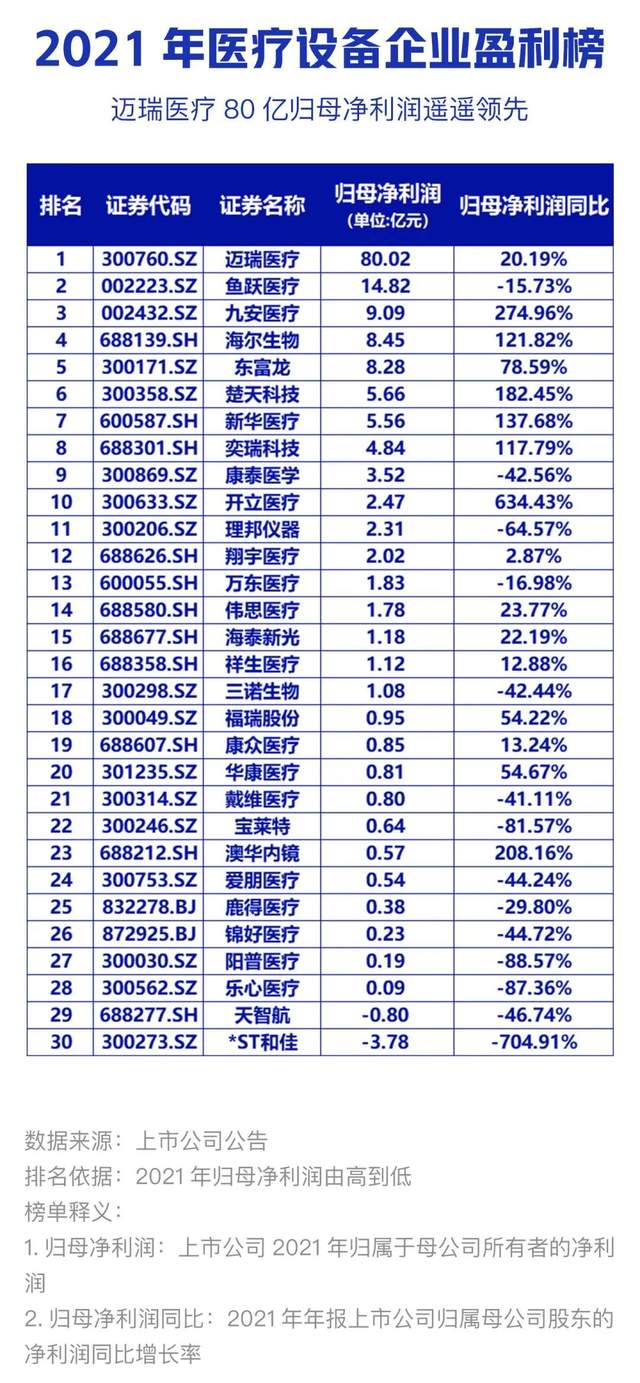
就在此前的3月26日,國務院新聞辦公室舉行的國務院政策例行吹風會上,國家藥品監督管理局副局長 徐景和最新介紹道:目前全國有醫療器械生產企業2.5萬多家,經營企業89.7萬多家。2019年全國醫療器械主營業收入達到7200多億元,約占全球醫療器械市場規模的20%。
2020年,國家多次組織聯合檢查組深入企業駐廠監督,強化檢查。加強產品抽檢和風險監測,督促企業落實主體責任,確保產品的質量安全。
并且,對于醫療器械相關單位、企業在生產經營過程中存在產品質量安全隱患,未及時采取有效措施消除的,監管部門應當對其進行約談,要求其限期改正。
日前,新修訂的《醫療器械監督管理條例》已經發布,新《條例》增加違法行為處罰到人制度,是近年來食品藥品監管領域立法的制度創新。
新《條例》有10余條規定,規定了對違法行為處罰到人。對違法單位處罰的同時,對違法單位的法定代表人、主要負責人以及直接負責的主管人員和其他責任人員,規定了財產罰、資格罰,沒收違法行為發生期間自本單位所獲收入,并處所獲收入最高3倍的罰款,禁止其五年直至終身不得從事醫療器械的生產經營活動。
此外,新《條例》還增設了醫療器械唯一標識追溯、網絡銷售管理、失信懲戒等制度,修改完善了醫療器械委托生產、上市后再評價等相關規定。
可以說,近年來對于醫療器械行業,國家正在逐步的貫徹“最嚴謹的標準、最嚴格的監管、最嚴厲的處罰、最嚴肅的問責”四個最嚴的要求。
據文件要求,新《條例》將于6月1日起正式施行。毫無疑問的是,隨著“四個最嚴”的逐步落實,全國范圍內的最強醫療器械監管也將開啟。
需要提醒的是,在國家的“組合拳”下,醫療器械全生命周期監管時代即將來臨......
本文來源:賽柏藍 作者:小編 免責聲明:該文章版權歸原作者所有,僅代表作者觀點,轉載目的在于傳遞更多信息,并不代表“醫藥行”認同其觀點和對其真實性負責。如涉及作品內容、版權和其他問題,請在30日內與我們聯系
 客服微v信:
客服微v信:







 京公網安備 11010802031568號
京公網安備 11010802031568號

