精彩內容 3月17日,國家藥監局官網顯示,江蘇奧賽康藥業的注射用右雷佐生以仿制3類提交上市申請獲批,并視同過評,是該產品首家過評企業。米內網數據顯示,2019年中國公立醫療機構終端右雷佐生注射劑銷售額超過7億元。 資料顯示,右雷佐生為蒽環藥物心臟毒性
精彩內容
3月17日,國家藥監局官網顯示,江蘇奧賽康藥業的注射用右雷佐生以仿制3類提交上市申請獲批,并視同過評,是該產品首家過評企業。米內網數據顯示,2019年中國公立醫療機構終端右雷佐生注射劑銷售額超過7億元。

資料顯示,右雷佐生為蒽環藥物心臟毒性保護劑,1992年首先在意大利上市,1995年7月獲美國FDA批準。
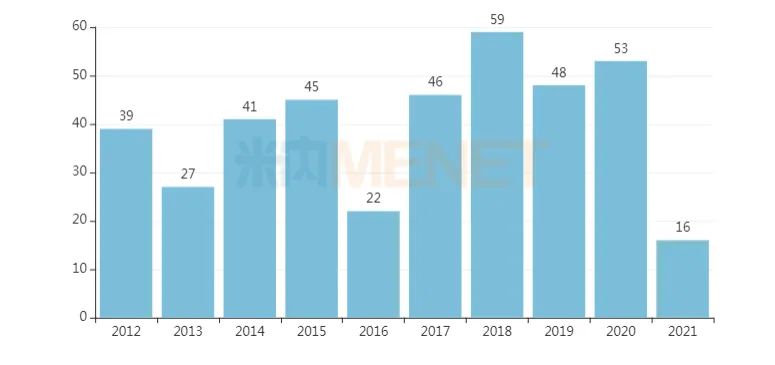
顯示,近年在中國城市公立醫院、縣級公立醫院、城市社區中心及鄉鎮衛生院(簡稱中國公立醫療機構)終端右雷佐生注射劑銷售額穩步增長,2019年超過7億元,生產廠家僅有江蘇奧賽康藥業一家。


來源:MED2.0中國藥品審評數據庫
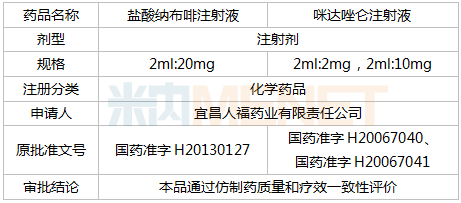
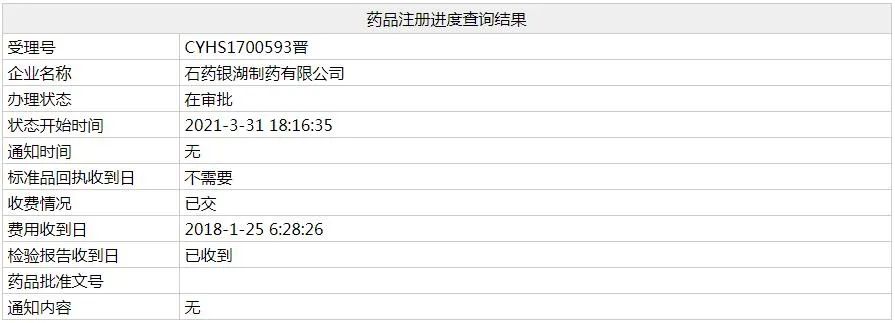
目前,江蘇奧賽康藥業此前獲批的注射用右雷佐生的一致性評價補充申請在審評審批中;上海凱茂生物醫藥|上海龍沙復星醫藥、南京正大天晴制藥均以仿制3類提交上市申請在審評審批中,獲批后視同過評。
資料來源:國家藥監局官網、米內網數據庫
本文來源:米內網 作者:白羽 免責聲明:該文章版權歸原作者所有,僅代表作者觀點,轉載目的在于傳遞更多信息,并不代表“醫藥行”認同其觀點和對其真實性負責。如涉及作品內容、版權和其他問題,請在30日內與我們聯系
 客服微v信:
客服微v信:








 京公網安備 11010802031568號
京公網安備 11010802031568號

